
“理想的疫苗”应该具有精确、微量、纯化、安全、高效的特点,不会对免疫系统造成负担,同时还应具备易于批量生产,易于储存运输,价格低廉的特征。为了实现这一目标,该研究提出通用的“头对尾”二聚体疫苗抗原模型。重组后的抗原显示了多对具有合适距离的表位,可以有效地激活B细胞。
以副粘病毒科新城疫病毒(NDV)的受体结合蛋白——血凝素神经氨酸酶蛋白(HN)为例,研究团队利用水稻胚乳表达系统成功制备了一种高效的重组抗原Osr2HN。研究结果显示,Osr2HN蛋白在水稻胚乳中正确表达,并且表达量高达3.7mg/g。晶体结构和小角X射线散射数据显示,重组后的Osr2HN蛋白形成了“蝴蝶状”的四聚体结构,具有完全暴露的受体结合域和中和表位。
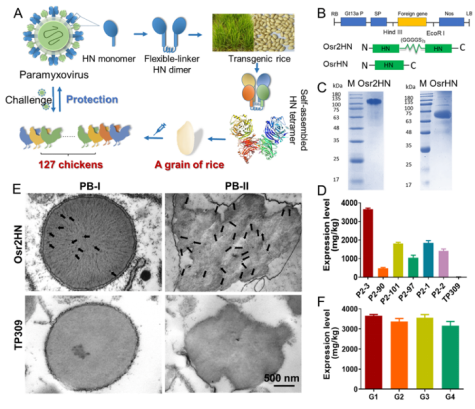
图1、Osr2HN的设计与表达
这些研究结果表明,水稻源的Osr2HN疫苗在安全性、高效性、低剂量和价格方面都取得了显著进展,达到了现代技术条件下疫苗产品所追求的最高境界。
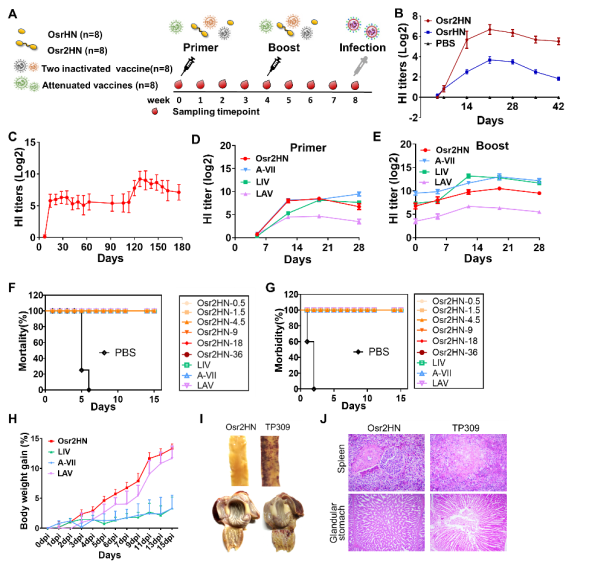
图2、Osr2HN完全保护鸡免受病毒攻击
马凡舒博士和许倩茹博士为本文的共同第一作者。河南农业大学、北京大学、龙湖现代免疫实验室的张改平院士,清华大学的饶子和院士及我院张二芹副教授为本文的共同通讯作者。本研究得到了河南省重大科技专项等项目的资助。
过去十余年,张改平院士团队一直致力于追求安全、高效、不浪费免疫潜力的“超级疫苗”,力争把疫苗做到现代科学技术条件下的最高境界。张改平院士表示“免疫潜力”的概念是指机体拥有巨大的免疫潜力,同时这种免疫潜力又是有限的。在正常情况下,机体生理能力是用于生长、抗逆、工作、学习和生产的。若过多用于免疫,会影响生产等能力,同时也因机体免疫系统承受压力过大而导致免疫保护效果欠佳。浪费免疫潜力的情况以往没有被高度重视。张改平院士认为,要在确保疫苗效果的同时尽量少使用免疫潜力,其根本是:“精确、微量、纯化、安全、高效”。精确即结构、位点、启动免疫反应的精确;微量即数个微克级,甚至是纳克级即可产生有效保护;纯化即尽可能地减少杂质;安全即实现真正的生物安全,无病原扩散;高效即占用动物极少的免疫潜力但能实现有效保护。
过去十余年,张改平院士团队一直致力于追求安全、高效、不浪费免疫潜力的“超级疫苗”,力争把疫苗做到现代科学技术条件下的最高境界。张改平院士表示“免疫潜力”的概念是指机体拥有巨大的免疫潜力,同时这种免疫潜力又是有限的。在正常情况下,机体生理能力是用于生长、抗逆、工作、学习和生产的。若过多用于免疫,会影响生产等能力,同时也因机体免疫系统承受压力过大而导致免疫保护效果欠佳。浪费免疫潜力的情况以往没有被高度重视。张改平院士认为,要在确保疫苗效果的同时尽量少使用免疫潜力,其根本是:“精确、微量、纯化、安全、高效”。精确即结构、位点、启动免疫反应的精确;微量即数个微克级,甚至是纳克级即可产生有效保护;纯化即尽可能地减少杂质;安全即实现真正的生物安全,无病原扩散;高效即占用动物极少的免疫潜力但能实现有效保护。
据悉,目前该疫苗已经于2023年8月与河南牧翔集团签约合作转让,此次转让实现了科技创新与产业发展的双向赋能,对于疫苗开发具有重大意义。(文/张二芹)
原文链接:https://doi.org/10.1073/pnas.2305745121
原文链接:https://doi.org/10.1073/pnas.2305745121
